Penemuan proton terjadi pada tahun 1815 saat ahli kimia yang berasal dari Inggris yaitu Willian Prout mengungkapkan bahwa semua atom terdiri dari atom hidrogen atau yang biasa disebut dengan protyles. Saat sinar kanal atau ion yang memiliki muatan positif dan dibentuk dari gas ditemukan oleh seorang fisikawan asal Jerman yaitu Eugen Goldstein di tahun 1886. Ia mengamati bahwa rasio dari muatan terhadap masa ion hidrogen merupakan yang paling tinggi di antara semua gas. Selain itu, Goldstein juga mengamati bahwa ion hidrogen mempunyai ukuran yang paling kecil diantara semua gas yang sudah terionisasi.
Inti atom tersebut ditemukan oleh Ernest Rutherford di tahun 1911 dalam penelitiannya terhadap kertas emasnya yang cukup terkenal. Ia menyimpulkan bahwa semua partikel memiliki muatan yang positif di dalam atom yang terkonsentrasi di inti tunggal dan sebagian besar volume di dalam atom kosong. Rutherford juga mengungkapkan bahwa jumlah total partikel yang bermuatan positif dalam inti yang sama dengan jumlah total elektron yang bermuatan negatif yang berada di sekitarnya.
Daftar Isi
Sejarah Penemu Proton dan Penemuan Proton
Apabila maa elektron berjumlah 0, maka suatu partikel tidak akan memiliki massa. Akan tetapi pada kenyataannya partikel materi memiliki massa yang bisa diukur dan atom tersebut bersifat netral. Bagaimana mungkin jika atom tersebut bersifat netral dan memiliki massa, apabila hanya ada elektron saja di dalam atomnya?
Adanya partikel yang bermuatan positif yang terkandung di dalam atom diisyaratkan oleh Eugen Goldstein sekitar tahun 1886. Dengan ditemukannya elektron, para ilmuan semakin percaya bahwa di dalam sebuah atom pasti ada partikel yang bermuatan positif dan berguna untuk mengimbangi muatan negatif dari elektron. Selain itu, apabila seandainya partikel penyusun atom hanyalah elektron, naka jumlah dari massa elektron akan lebih kecil dibandingkan dengan massa sebutir atom.
Pada tahun 1886, Goldstein juga melakukan sebuah eksperimen menggunakan tabung gas yang mempunyai katode dan sudah diberi lubang-lubang kemudian dialiri muatan listrik. Setelah itu, gas yang ada di belakang katode menjadi menyala. Peristiwa tersebut menunjukkan bahwa ada radiasi yang berasal daro anode yang menerobos ke dalam lubang yang ada di lempeng katode. Sinar itu disebut denga sinar anode atau sinar yang bersifat positif. Sifat dari sinar anode yaitu:
a. Sinar anode adalah radiasi partikel, jadi bisa memutar sebuah baling-baling
b. Di dalam medan listrik atau magnet, dibelokkan ke kutub negatif, jadi sinar anode termasuk ke dalam radiasi bermuatan positif
c. Partikel yang ada di dalam sinar anode bergantung pada jenis gas yang ada di dalam tabung
Hasil dari eksperimen tersebut ternyata dapat membuktikan bahwa pada saat proses terbentuknya elektron menuju anode, akan terbentuk juga sinar positif yang menuju ke arah berlawanan melewati lubang yang ada di katode. Setelah berbagai macam gas dicoba di masukkan ke dalam tabung tersebut, ternyata gas hidrogenlah yang bisa menghasilkan sinar bermuatan positif terkecil baik massanya atau muatannya. Sehingga partikel itu disebut dengan Proton. Massa proton sama dengan 1 sma atau satuan massa atom dan muatan proton sama dengan +1.
Kehadiran partikel penyusun atom yang bermuatan positif semakin terbukti saat Ernest Rutherford, seseorang yang berasal dari Selandia Baru pindah ke Negara Inggris di tahun 1906 bersama kedua asistennya, yang bernama Hans Geiger dan Ernest Marsden. Mereka kemudian melakukan serangkaian eksperimen untuk mengetahui kedudukan patikel yang ada di dalam atom. Eksperimen mereka dikenal sebagai hamburan sinar alfa pada lempeng tipis emas. Mereka kemudian berhasil menghitung bahwa massa pada partikel bermuatan positif itu diperkirakan 1.837 kali massa elektron. Sekarang kita menyebutnya dengan sebuatan proton. Istilah tersebut baru saja digunakan mulai tahun 1919.
Massa 1 elektron = 9,11 × 10–28 gram
Massa 1 proton = 1.837 × 9,11 × 10–28 gram = 1,673 × 10–24 gram
Dari pengatam ketiganya, diperoleh sebuah fakta bahwa partikel α yang ditembakkan kepada lempeng logam emas tipis, sebagai besar akan diteruskan dan sebagian lainnya akan dibelokkan. Bahkan ada juga sebagian yang dipantulkan. Hal itu cukup mengejutkan bagi Rutherford. Penemuannya menyebabkan teori atom Thomson gugur. Di dalam eksperimennya, partikel α yang terpantul diperkirakan sudah menabrak sesuatu yang padat dalam atom. Dengan begitu, atom tersebut tidak bersifat homogen seperti yang telah digambarkan oleh Thomson. Bahkan menurut Marsden, terdapat fakta bahwa satu diantara 20.00 partikel α akan berbelok dengan sudut 90 derat atau bahkan bisa lebih.
Berdasarkan gejala yang sudah dijelaskan di atas, didapatkan beberapa kesimpulan diantaranya:
a. Atom tidak merupakan bola pejal. Sebab hampir semua partikel yang ada di dalamnya adalah alfa (α) yang diteruskan. Itu artinya, sebagian besar volume atom adalah ruang kosong.
b. Partikel yang mengalami pembelokan adalah partikel α yang sudah mendekati inti atom. Hal itu disebabkan karena keduanya memiliki muatan positif.
c. Partikel yang dipantulkan adalah partikel α yang sudah menabrak inti atom.
Berdasarkan fakta yang diperoleh dari eksperimen tersebut, Rutherford mengusulkan modal atom yang Ia temukan dan menyatakan bahwa atom terdiri dari initi atom yang sangat kecil dan memiliki muatan positif dan dikelilingi oleh elektron yang bermuatan negatif. Jumlah proton yang ada di dalam inti sama dengan jumla elektron yang mengelilingi inti. Sehingga atom memiliki sifat yang netral. Rutherford juga menganggap bahwa di dalam inti atom ada partikel netral yang berfungsi untuk mengikat partikel positif supaya tidak saling menolak. Dari eksperimen tersebut, Rutherford bisa memperkirakan jari-jari atom yaitu kira-kira 10–8 cm dan jari-jari intinya kira-kira 10–13 cm.
Apa Itu Proton?
Proton adalah salah satu jenis partikel subatomik, dimana partikel tersebut adalah partikel minimum yang membentuk sebuah atom. Selain itu, proton juga termasuk ke dalam keluarga fermion yang dilengkapi dengan adanya muatan listrik yang bersifat positif. Semua materi umumnya terbuat dari atom dan setiap gilirannya terdiri dari tiga jenis partikel yang berbeda, serta dilengkapi dengan tiga jenis muatan listrik, antara lain:
1. Elektron yang bermuatan negatif
2. Neutron yang bermuatan netral
3. Proton yang bermuatan positif
Karakteristik Proton
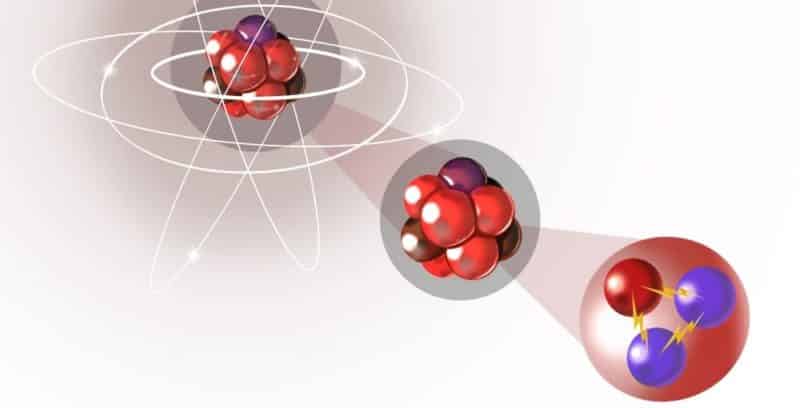
Proton adalah partikel komposit yang bersifat stabil dan jauh lebih besar dibandingkan elektron yaitu 1.836 kali seperti yang sudah dijelaskan di atas. Selain itu, proton juga dianugrahi muatan elementer yang bersifat positif 1 (1,6 x 10^-19 C). Disisi lain, proton sendiri tersusun dari tiga partikel dasar. Waktu paruh dari proton lebih besar daripada 1035 tahun, dimana proton sangat rentan terhadap suatu peluruhan. Lalu, proton juga memiliki partikel subatomik lainnya dan putarannya sendiri. ini adalah momentum sudut intrinsil dan tidak bisa berubah-ubah dan di dalamnya yaitu 1/2. Sifat tersebut sangatlah berguna untuk resonansi magnetik nuklir dan juga digunakan untuk aplikasi teknologi modern lain.
Struktur Proton
Proton dan juga neutron mempunyai strukturnya masing-masing. Di dalam proton dan juga neutron, kita bisa menemukan partikel elementer yang bersifat kekal. Partikel tersebut biasa disebut dengan quark. Di dalam intinya, proton dan juga neutron terhubung melalui kekuatan yang cukup besar, yaitu berupa interaksi yang bertugas untuk mengatur perilaku quark dan membentuk proton serta neutron individu. Protong seringkali disebut memiliki komposisi quark yang berasal dari uud. Sehingga bilangan kuantum memiliki muatan sebagai berikut:
q (uud) = ⅔ + ⅔ + (-1/3) = +1
Massa dari proton di atas adalah 938.272 MeV / c2. Sedangkan untuk massa ketiga quark hanya berkisar 12 MeV / c2 yaitu hanya sekitar 1 persen dari energi massa neutron. Sama halnya proton, sebagian besar dari massa atau energi yang berasal dari neutron berbentuk energi gaya nuklir yang cukup kuat (gluon) Quark neutron kemudian disatukan dengan gluon yaitu partikel penukar untuk gaya nuklir yang kuat.
Stabilitas Proton
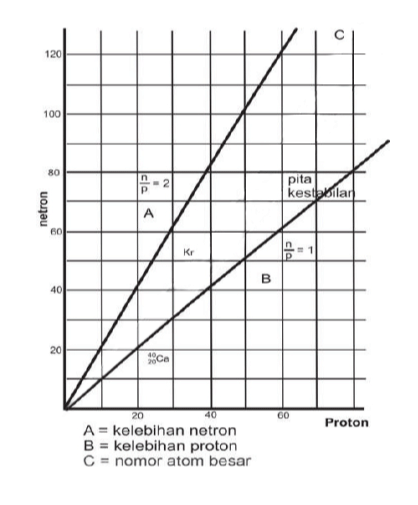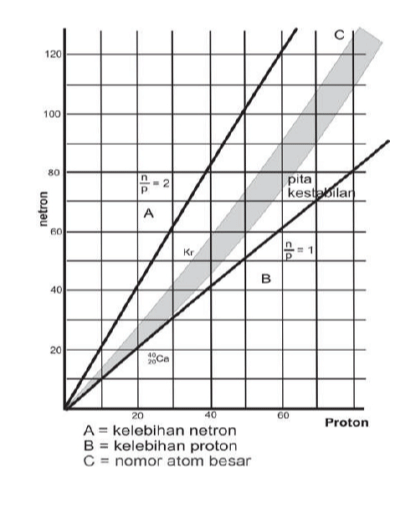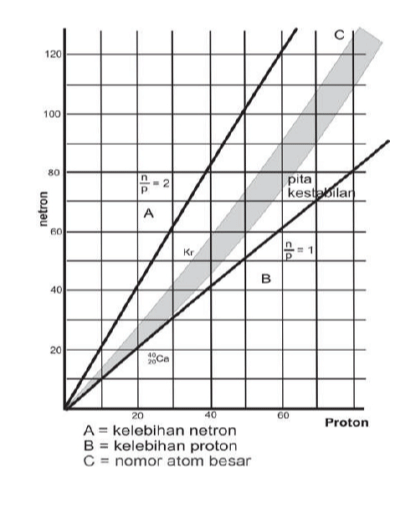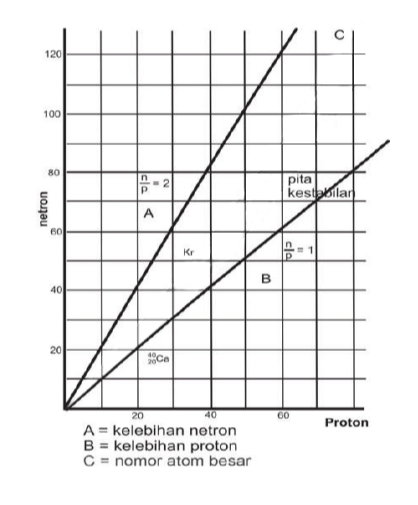
Proton bebas atau proton yang tidak lagi terikat dengan nukleon atau elektron adalah partikel stabil yang belum diteliti untuk terurai secara spontan ke partikel lainnya. Selain itu, proton bebas tersebut ditemukan secara alami yaitu di dalam sejumlah situasi dan kondisi. Misalnya saja proton bebas membentuk 90 persen sinar kosmik. Dimana energi atau suhunya yang cukup tinggi bertugas untuk memisahkannya dari elektron yang memiliki afinitas. Peluruhan proton juga dihubungkan dengan hukum kekekalan nomor baryon. Nomor Baryon adalah sebuah generalisasi nomor nukleon yang dikonservasi di dalam reaksi dan juga peluruhan nuklir non relativistik.
Hukum tersebut menyatakan bahwa:
Jumlah bilangan pada nomor baryon yang berasal dari seluruh partikel yang masuk adalah sama dengan jumlah bilangan pada nomor baryon yang berasal dari semua partikel yang dihasilkan dari reaksi.
Inti atom
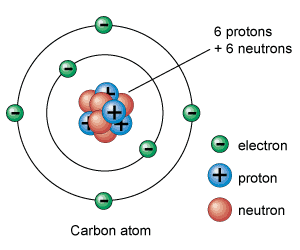
Proton biasanya ditemukan pada inti atom, proton, dan neutron. Dimana ketiganya seringkali disebut dengan nukleon. Disisi lain, elektron mengorbit di sekitar ketiga partikel tersebut dengan cara menyebar. Kemudian inti atom tersebut dikaitkan dengan gaya nuklir yang cukup kuat. Dimana di dalam kasus atom-atom yang besar seperti halnya Uranium, mereka bisa menghasilkan gaya lain, seperti elektromagnetik. Nukleon tersebut merupakan persentase tertinggi dari sebuah massa atom apapun. Karenanya, mereka bisa menentukan perbedaan antara unsur kimia dan unsur lainnya. Seperti misalnya, atom hidrogen yang hanya memiliki satu proton di dalam intinya. Sementara helium mempunyai dua proton dan juga satu atau dua neutron, bergantung dengan isotop spesifik.
Nomor Atom
Nomor atom yang ada pada tiap-tiap unsur bisa dilihat pada tabel periodik. Dimana nomor atom Z biasanya menunjukkan seberapa banyak proton yang ada di dalam suatu jenis atom dalam nukleusnya. Pada tiap unsur kimianya memiliki nomor atom yang berbeda-beda. Meskipun perilaku mereka juga sama-sama ditentukan oleh jumlah elektron yang mengorbit di bagian inti. Sehingga, misalnya klorin (CI) memiliki 17 proton di dalam nukleusnya. Maka nomor atomnya juga berjumlah 17. Angka tersebut tidak pernah bervariasi, bahkan di antara isotop dari versi atom yang sama. Hal tersebut disebabkan karena mereka memiliki jumlah neutron yang berbeda pada intinya.
Muatan dan Massa Proton
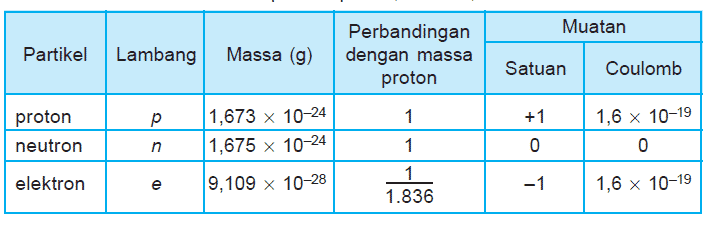
Di dalam ilmu fisika, proton adalah suatu partikel subatomik yang bermuatan positif sebesar 1.6 × 10-19 coulomb dan juga memiliki massa sebesar 938 MeV (1.6726231 × 10-27 kg, atau sekitar 1.836 kali massa dari elektron. Sebuah atom biasanya terdiri dari sejumlah proton dan juga neutron yang ada di bagian inti atom, dan juga sejumlah elektron yang mengelilingi inti atom tersebut. Di dalam atom yang bermuatan netral, jumlah proton tersebut akan sama dengan jumlah elektronnya. Dimana jumlah proton di bagian inti biasanya akan bertugas untuk menentukan sifat kimia dari suatu atom. Inti dari atom tersebut seringkali disebut dengan nama nukleus, nuklei, dan juga nukleon. Kemudian reaksi yang terjadi atau yang berkaitan dengan inti atom tersebut akan disebut sebagai reaksi nuklir.
Sifat fisik
Proton biasanya memiliki massa yang lebih sedikit dibandingkan dengan neutron yang ada di dalam inti. Namun mereka 1.836 kali lebih besar daripada elektron. Massa aktual dari proton adalah 1,6726 x 10 ^ -27 kilogram. Itu adalah salah satu massa yang sangat kecil. Simbol “^ -” akan mewakili eksponen negatif. Angka tersebut adalah titik desimal yang diikuti oleh 26 nol, maka angkanya menjadi 16.726. Di dalam muatan listrik tersebut, proton berubah menjadi positif, bukan lagi sebagai partikel dasar. Justru proton tersebut sebenarnya terdiri dari tiga partikel kecil yang biasanya disebut dengan quark.
Fungsi dalam Atom
Proton yang ada di dalam inti atom bertugas untuk membantu dalam mengikat inti secara bersamaan. Selain itu, proton juga akan menarik elektron yang bermuatan negatif. Dimana jumlah proton yang ada di dalam inti atom tersebut akan menentukan unsur kimianya. Angka tersebut dikenal sebagai nomor atom atau seringkali dilambangkan dengan huruf kapital Z.
Energi untuk Bintang
Di dalam matahari dan juga seluruh bintang lainnya, proton tersebut bergabung dengan proton lainnya melalui fusi nuklir. Namun fusi tersebut masih memerlukan suku yang tinggi yaitu 1 juta derajat celcius. Suhu tersebut akan menyebabkan dua partikel yang lebih ringan melebur menjadi partikel ketiga. Massa dari partikel tersebut kurang dari dua partikel awal yang digabungkan. Albert Einstein pada tahun 1905 menemukan suatu hal yaitu materi dan juga energi bisa dikonservasi dari satu bentuk ke bentuk lainnya. Hal itu menjelaskan tentang bagaimana hilangnya massa pada saat proses fusi muncul yang merupakan energi dari pancaran bintang.
Contoh Proton
Perlu dipahami bahwa proton bebas itu nyata adanya. Inti dari atom hidrogen dan juga ion H + adalah contoh dari proton bebas. Terlepas dari isotop, setiap atom hidrogen akan memiliki satu proton. Kemudian setiap atom helium akan memiliki dua proton dan setiap atom litium akan mengandung tiga proton dan seterusnya.
Demikian penjelasan lengkap mengenai penemu proton, sejarah, pengertian, struktur, sifat, dan lainnya. Untuk Grameds yang tertarik untuk belajar ilmu fisika atau ilmu kimia secara lebih dalam, maka materi ini juga perlu dipahami dan dipelajari ya. Supaya pengetahuan ilmu fisika dan kimianya bisa bertambah. Semoga artikelnya mudah dipahami ya.
- Galileo Galile
- Penemu Telepon
- Penemu Lampu Pijar
- Penemu Arus Listrik
- Penemu Termometer
- Penemu Jam
- Penemu Facebook
- Penemu Sel
- Penemu Proton
- Penemu Baterai
- Penemu Program Pascal
- Penemu Aljabar dan Algoritma
- Penemu Sepeda
- Penemu Kamera
- Penemu Televisi
- Penemu Mesin Uap
- Penemu Not Balok
- Penemu Sandi Morse
- Penemu Handphone
- Penemu Internet
- Penemu Wifi
- Penemu Google
- Penemu Komputer
- Penemu Microsoft
- Penemu Angka Nol
- Penemu Matematika
- Penemu Teleskop
- Penemu Mobil
- Penemu Pesawat Terbang
- Penemu Inti Atom
- Penemu Permainan Bola Basket
- Penemu Benua Australia
- Penemu Copy Paste
- Penemu Permainan Bola Voli
- Penemu Permainan Sepak Bola
- Penemu Benuar Amerika











