Persamaan Reaksi – Perkembangan ilmu pengetahuan kimia terus mengalami kemajuan, bahkan bisa dikatakan bahwa tanpa adanya perkembangan ilmu pengetahuan kimia, dunia ini akan terasa membosankan. Hal ini disebabkan karena adanya reaksi kimia pada kehidupan sehari-hari. Umumnya reaksi kimia ini sudah sering terjadi pada diri kita, yaitu pada saat makan yang di mana makanan yang kita makan akan berubah menjadi energi. Reaksi kimia juga bisa terjadi pada besi yang bisa berubah menjadi karat.
Reaksi kimia yang terjadi hampir pada kehidupan kita sehari-hari ini merupakan interaksi antara dua komponen dasar yang berasal dari alam semesta, yaitu energi dan materi. Energi adalah suatu kemampuan untuk membentuk ulang beberapa materi. Sedangkan materi adalah setiap zat yang ada ada yang berfungsi untuk mengisi ruang. Dengan adanya energi dan materi tersebut, maka akan terjadi suatu perubahan yang bisa menciptakan zat baru.
Dalam ilmu pengetahuan kimia, terjadinya reaksi kimia bisa dibilang sebagai kajian utama dari ilmu pengetahuan kimia itu sendiri. Setiap zat yang terlibat dalam terjadinya reaksi kimia akan terlihat sulit dijelaskan karena terdiri dari banyak sekali lambang. Oleh sebab itu, supaya reaksi kimia mudah dipahami, maka akan dinyatakan ke dalam bentuk persamaan reaksi.
Maka dari itu, kalau berbicara tentang reaksi kimia, maka tidak akan lepas dari persamaan reaksi kimia. Hampir semua para ahli kimia menulis persamaan kimia agar dapat menjelaskan hal-hal yang muncul selama reaksi kimia terjadi. Dengan adanya persamaan reaksi, maka informasi yang diberikan ketika terjadi reaksi kimia akan lebih lengkap.
Persamaan reaksi ditulis secara detail dengan memasukkan setiap simbol, huruf, dan angka. Simbol yang ada pada persamaan reaksi bisa dibilang cukup penting karena bermanfaat untuk memberikan tambahan informasi tentang cara agar reaksi kimia berjalan dengan baik. Persamaan reaksi yang dapat menjelaskan terjadinya reaksi kimia, didalamnya terdapat beberapa hal, seperti rumus kimia zat-zat pereaksi dan zat-zat hasil reaksi yang diikuti dengan koefisien dan fasa masing-masing.
Memang untuk menulis persamaan reaksi akan terlihat sulit bagi yang belum terbiasa, sehingga dibutuhkan langkah-langkah menulis persamaan reaksi. Bagi kamu yang ingin mengetahui langkah-langkah menulis persamaan reaksi bisa membaca artikel ini. Di dalam artikel ini akan dibahas juga tentang pengertian dari persamaan reaksi. Jadi, bca artikel ini sampai habis, Grameds.
Daftar Isi
 Pengertian Reaksi
Pengertian Reaksi
Persamaan reaksi adalah suatu pernyataan yang ditulis dengan memakai rumus-rumus kimia yang di mana berfungsi untuk memberikan informasi tentang kuantitas dan identitas dari suatu zat yang ada di dalam suatu reaksi kimia. Selain itu, persamaan reaksi bisa juga diartikan sebagai salah satu cara untuk memperlihatkan adanya hubungan antara zat-zat kimia yang ada sebelum dan sesudah reaksi kimia.
Persamaan reaksi dapat ditulis atau dinyatakan dengan menggunakan rumus kimia dari zat-zat yang bereaksi dan hasil reaksi, yaitu angka koefisien dan wujud zat atau fasa. Di dalam persamaan reaksi, setiap simbol dan setiap rumus yang digunakan akan mewakili setiap materi dan mewakili produk atau hasil reaksi. Materi yang ada pada persamaan reaksi ditulis pada bagian kiri. Sedangkan produk (hasil reaksi) pada persamaan reaksi ditulis di sebelah kanan.
Adanya dua sisi pada penulisan persamaan reaksi menandakan bahwa persamaan reaksi berbeda dengan tata nama senyawa. Tanpa adanya dua sisi ini, kita akan sulit menentukan mana pereaksi (reaktan) dan mana hasil reaksi (produk).
Tidak hanya itu, ketika kamu ingin menulis persamaan reaksi pasti menggunakan tanda panah. Di dalam persamaan reaksi, tanda panah berfungsi sebagai tanda reaksi kimia, yaitu “reaktan” dan “membentuk produk” atau bisa juga diartikan seperti “membentuk” dan “bereaksi menjadi”.
Selain tanda panah, dalam penulisan persamaan reaksi biasanya diberikan informasi terkait dengan kondisi fisik dari senyawa. Kondisi fisik pada senyawa yang biasa digunakan ada empat, yaitu solid, liquid, dan gas. Solid memiliki simbol “s”, liquid memiliki simbol “l”, aqueous memiliki simbol “aq”, dan gas memiliki simbol “g”.
Di dalam persamaan reaksi terdapat bilangan yang mendahului rumus kimia zat-zat dan bilangan-bilangan tersebut disebut dengan istilah koefisien reaksi. Diberikannya koefisien reaksi pada persamaan reaksi berfungsi untuk melakukan penyetaraan atom-atom sebelum dan sesudah reaksi kimia. Selain itu, koefisien reaksi bukan hanya bisa dapat menyetarakan persamaan reaksi saja, tetapi koefisien reaksi bisa menyatakan suatu perbandingan yang sangat sederhana dari setiap partikel zat-zat yang ada di dalam suatu reaksi kimia.
Hal yang perlu kamu ketahui ketika menulis persamaan reaksi adalah setiap zat yang berada dalam sebuah reaksi kimia, maka jumlah atom pada zat tersebut akan berkurang. Dengan kata lain, proses reaksi bisa menyebabkan atom dalam suatu zat berkurang. Proses reaksi sering dikenal dengan istilah pereaksi (reaktan).
Syarat Persamaan Reaksi
Persamaan reaksi sempurna adalah persamaan reaksi yang setara. Untuk menulis persamaan reaksi yang setara, maka perlu memerhatikan syarat persamaan reaksi. Dikutip dari Kementerian Pendidikan dan Kebudayaan Republik Indonesia, terdapat syarat-syarat persamaan reaksi setara, di antaranya:
1. Jenis unsur-unsur sebelum dan sesudah dilakukan persamaan reaksi sempurna harus selalu sama.
2. Jumlah dari setiap atom sebelum dan reaksi harus selalu sama (memenuhi hukum kekekalan massa).
3. Setiap perbandingan dari koefisien reaksi menyatakan perbandingan mol. Namun, khusus zat yang wujudnya berupa gas, maka perbandingan koefisien juga menyatakan perbandingan volume apabila suhu dan tekanannya sama.
4. Pereaksi dan hasil reaksi harus dinyatakan dengan memakai rumus kimia yang benar.
5. Setiap dari wujud zat yang ada pada reaksi harus dinyatakan dengan menggunakan tanda kurung sesudah rumus kimia.
Pada dasarnya, untuk menulis persamaan reaksi sempurna atau persamaan reaksi setara sebenarnya bisa dengan cara mengubah jumlah rumus kimia (satuan rumus atau jumlah molekul). Meskipun bisa mengubah jumlah rumus kimia, tetapi dari perubahan itu tidak bisa mengubah rumus kimia zat-zat yang terkait dalam persamaan reaksi.
 Hal yang Harus Ada pada Persamaan Reaksi
Hal yang Harus Ada pada Persamaan Reaksi
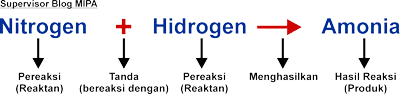
Secara garis besar, di dalam persamaan reaksi ada 4 hal yang harus ada, yaitu reaktan, produk (hasil reaksi), tanda persamaan, dan jumlah koefisien. Supaya keempat hal tersebut lebih jelas, maka di bawah ini akan dijelaskan lebih lanjut.
1. Reaktan (Pereaksi)
Reaktan adalah zat kimia yang ada di dalam suatu persamaan reaksi dan selalu mengalami reaksi. Reaktan sering disebut juga dengan istilah pereaksi dan letak dari pereaksi ada di bagian sebelah kiri dari persamaan reaksi. Dengan kata lain, reaktan atau pereaksi tidak pernah berada di bagian kanan dari persamaan reaksi. Hal ini dikarenakan zat kimia yang ada di sebelah kanan sudah bukan lagi reaktan atau pereaksi.
2. Produk (Hasil Reaksi)
Produk adalah zat atau senyawa kimia yang dihasilkan dari proses suatu reaksi kimia. Berbeda dengan reaktan (pereaksi) yang letaknya berada di bagian kiri persamaan reaksi, produk terletak pada bagian kanan dari persamaan reaksi. Produk sering disebut dengan hasil reaksi, sehingga tanpa adanya produk (hasil reaksi), maka tidak akan terjadi persamaan reaksi.
blogmipa-kimia.blogspot.com
3. Tanda Persamaan
Hal ketiga yang harus ada pada persamaan reaksi adalah tanda persamaan. Tanda persamaan yang ada di persamaan reaksi ada dua tanda, yaitu tanda tambah (+) dan tanda panah (→). Bukan hanya harus ada, tetapi dalam penulisannya, tanda persamaan ini letaknya tidak boleh salah atau tertukar karena jika salah, maka fungsinya akan berbeda.
Tanda tambah (+) berfungsi untuk menjadi pemisah satu reaktan dengan reaktan lainnya. Sementara itu, tanda (→) berfungsi untuk menjadi pemisah antara reaktan (pereaksi) dengan produk (hasil reaksi).
4. Jumlah Koefisien
Jumlah koefisien adalah angka atau nomor yang ada pada reaktan (pereaksi) dan produk (hasil reaksi) dan terletak pada bagian kiri dari senyawa atau zat kimia. Dalam menentukan koefisien reaksi, jika tidak ada nomor pada bagian sebelah kiri senyawa atau zat kimia, maka koefisien reaksi tersebut akan dianggap 1. Hal seperti itu sudah menjadi ketentuan pasti dalam persamaan reaksi.
Jadi, ketika kamu ingin menulis persamaan reaksi, maka harus dipastikan bahwa keempat hal itu harus ada. Jika, salah satu dari keempat hal itu tidak ada, maka belum bisa dikatakan sebagai persamaan reaksi.
blogmipa-kimia.blogspot.com
Wujud Zat Persamaan Reaksi
Di dalam persamaan reaksi kimia bukan hanya menjelaskan tentang perubahan senyawa atau zat kimia saja, tetapi juga memperlihatkan wujud-wujud zat yang ada di dalamnya. Setiap wujud zat kimia yang terlibat di dalam persamaan reaksi memiliki notasi wujudnya masing-masing, di antaranya:
Solid
Solid merupakan zat kimia yang bersifat atau bentuknya berupa zat padat. Setiap zat yang bersifat padat, maka akan dinotasikan atau disimbolkan dengan huruf (s).
Liquid
Liquid adalah zat kimia yang bersifat atau bentuk dari zat tersebut berupa zat cair. Oleh sebab itu, setiap zat cair akan dimasukkan ke dalam kategori wujud zat liquid dan dinotasikan atau disimbolkan dengan huruf (l).
Aqueous
Aqueous adalah zat kimia yang berupa larutan dalam air. Pada wujud zat ini akan dinotasikan atau disimbolkan dengan huruf (aq).
Gas
Gas adalah wujud zat yang di mana setiap molekulnya dapat bergerak bebas, sehingga dapat menempati semua volume. Wujud zat kimia yang satu ini di dalam persamaan reaksi memiliki notasi wujud atau diberi simbol dengan huruf (g).
 Cara Menulis Persamaan Reaksi
Cara Menulis Persamaan Reaksi
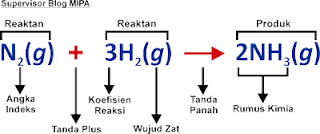
Dalam menulis persamaan reaksi, ada hal yang perlu digarisbawahi, yaitu penulisan indeks. Indeks dalam rumus kimia adalah suatu angka yang di mana ketika menulisnya memakai format subscript. Subscript adalah penulisan angka berukuran kecil yang terletak pada bagian kaki huruf. Sementara itu, ketika menulis persamaan reaksi, indeks ditulis di bagian kanan bawah. Langkah-langkah menulis persamaan reaksi, yaitu:
Langkah Pertama
Kamu harus tulis persamaan reaksi dalam kata-kata terlebih dahulu. Persamaan reaksi yang ditulis harus terdiri dari wujud zat dan nama zat yang berasal dari reaktan (pereaksi) dan produk (hasil reaksi).
Langkah Kedua
Setelah menulis reaktan (pereaksi) dan produk (hasil reaksi), maka Langkah berikutnya, kamu harus menerjemahkan setiap persamaan reaksi yang sudah ditulis dengan kata-kata ke dalam bentuk rumus kimia. Adapun rumus kimia yang ditulis harus sesuai dengan masing-masing senyawa atau zat kimia. Selain itu, kamu juga harus memberikan keterangan dari wujud zat tersebut.
Langkah Ketiga
Melakukan penyetaraan terhadap persamaan reaksi dengan cara memberikan koefisien yang sesuai dengan penyetaraan tersebut.
Supaya kamu lebih mudah untuk memahami setiap langkah menulis persamaan reaksi, maka di bawah ini akan digambarkan cara menulis persamaan reaksi.
1. Persamaan kata-kata yang terdiri dari aluminium oksida padat + larutan asam klorida → larutan aluminium klorida + air
2. Penulisan zat kimia dengan rumus kimia, Al2O3(s) + HCl(aq) → AlCl3(aq) + H2O(l). pada penulisan zat kimia tersebut belum disetarakan.
3. Persamaan reaksi setara menghasilkan, Al2O3(s) + 6HCl(aq) → 2AlCl3(aq) + 3H2O(l).
Dari contoh langkah menulis persamaan reaksi di atas, maka dapat disimpulkan bahwa suatu persamaan reaksi bisa dibilang setara, jika jumlah dari setiap atom dari zat-zat reaktan (pereaksi) yang ada di sebelah kiri sama dengan zat-zat produk (hasil reaksi) yang ada di sebelah kanan.
Cara Menyetarakan Persamaan Reaksi
Penyetaraan persamaan reaksi perlu dilakukan agar hasil dari persamaan reaksi bisa setara. Cara menyetarakan persamaan reaksi sebagai berikut.
Langkah Pertama
Menulis koefisien reaksi yang dinyatakan dalam bentuk (contoh, a, b, c, dan d) di setiap zat kimia.
Langkah Kedua
Melakukan penyusunan terhadap persamaan matematis yang sesuai dengan kesamaan dari jumlah atom dan unsur yang sama yang ada di sebelah kiri atau di sebelah kanan.
Langkah Ketiga
Melakukan penyelesaian terhadap persamaan matematis yang didapatkan dari langkah kedua. Dalam menyelesaikan persamaan matematis ini, kamu harus menentukan koefisien dari salah satu zat yang memiliki rumus kimia yang paling kompleks.
 Contoh Persamaan Reaksi
Contoh Persamaan Reaksi
Pada umumnya hampir semua zat kimia bisa menciptakan persamaan reaksi, sehingga contoh dari persamaan reaksi sangatlah banyak. Di bawah ini akan diberikan beberapa contoh dari persamaan reaksi.
Contoh Pertama
Persamaan reaksi gas hidrogen yang akan bereaksi dengan gas oksigen dan menghasilkan produk berupa zat air.
H2O(g) + O2(g) → H2O(l)
Contoh Kedua
Persamaan reaksi asam nitrat dengan gas hidrogen sulfida dan produknya nitrogen oksida, sulfur, dan air.
HNO3(aq) + H2S(g) → NO(g) + S(s) + H2O(l)
Contoh Ketiga
Persamaan reaksi kalium hidroksida dengan larutan asam fosfat yang kemudian menghasilkan produk larutan kalium dan air.
KOH(aq) + H3PO4(aq) → K3PO4(aq) + H2O(l)
Contoh Keempat
Persamaan reaksi aluminium dengan larutan asam nitrat, kemudian menghasilkan produk larutan alumunium nitrat, air, dan gas nitrogen dioksida.
3KOH(aq) + H3PO4(aq) → K3PO4(aq) + 3H2O(l).
Kesimpulan
Persamaan reaksi akan memudahkan seseorang mengenal zat-zat apa saja yang ada pada saat terjadinya reaksi kimia. Selain itu, persamaan reaksi bisa menentukan kemungkinan zat-zat yang akan dihasilkan dari reaksi kimia yang telah terjadi. Dengan demikian, dapat dikatakan bahwa persamaan reaksi memiliki fungsi utama yaitu menjelaskan tentang reaksi kimia yang sedang terjadi.
Pada persamaan reaksi, ada empat hal yang perlu kamu perhatikan, yaitu reaktan, produk, tanda persamaan, dan jumlah koefisien. Reaktan sering disebut juga pereaksi yang letaknya ada di sebelah kiri persamaan reaksi. Kemudian, produk biasa juga disebut dengan istilah hasil reaksi dan letaknya ada di sebelah kanan pada persamaan reaksi. Dengan persamaan reaksi juga, seseorang bisa mengetahui jumlah perbandingan dari setiap senyawa atau zat kimia yang ada didalamnya.
Rekomendasi Buku & Artikel Terkait
- Asam dan Basa
- Benzoil Peroksida
- Hukum Hess
- Kimia
- Jenis-jenis Indikator Asam Basa
- Niacinamide
- Teori Atom Mekanika Kuantum
- Pengertian Konsentrasi Larutan dan Satuan-satuannya
- Perkembangan Teori Atom dan Tokoh-Tokohnya
- Tabel Periodik: Pengertian, Unsur, Klasifikasi, Dan Cara Membacanya
- Contoh Campuran Heterogen & Ciri Campuran Heterogen
- Contoh Campuran Homogen & Bedanya Campuran Heterogen
- Perbedaan Senyawa dan Campuran
- Pengertian, Sifat, Jenis, dan Contoh Senyawa
- Pengertian Kesetimbangan Kimia
- Pengertian Reaksi Kimia
- Pengertian Energi Kimia
- Pengertian Perubahan Kimia
- Pengertian Polimer
- Pengertian Eksoterm & Endoterm
- Persamaan Reaksi
- Radioaktif
- Rumus Empiris
- Teori Asam Basa
- Contoh Asam Kuat dan Asam Lemah
- Contoh Basa
- Titanium
- Pengertian Energi Alternatif
- Sifat Koligatif Larutan
- Zat Campuran
- Laju Reaksi
- Rumus Hukum Faraday
- Rumus Molekul
- Rumus Derajat Ionisasi
- Proses Korosi dan Pencegahannya
- Contoh Larutan Elektrolit
- Tata Nama Alkana
- Contoh Mengkristal
- Massa Jenis Minyak
- Fraksi Minyak Bumi
Sumber: Dari berbagai macam sumber











