Pengertian Atom dan Perkembangan Atom – Pada dasarnya, setiap material yang ada di dunia ini pasti mempunyai bagian yang paling kecil, lalu jika bagian kecil itu dibelah lagi, maka akan terdapat bagian yang lebih kecil lagi. Nah, bagian kecil dari bagian yang terkecil itulah disebut dengan atom.
Atom itu sendiri bisa dikatakan sebagai penyusun materi terkecil dari segala materi yang ada. Secara sederhana atom bisa diartikan seperti itu. Selain itu, dalam dunia sains, atom memiliki perkembangannya. Setiap perkembangan pada atom merupakan hasil evaluasi dari teori atom sebelumnya.
Ingin tahu penjelasan lebih lengkap tentang pengertian atom dan ingin tahu perkembangan atom? Tunggu apalagi, langsung baca artikel ini, maka kamu akan mengetahui pengertian dan perkembangan atom.
Daftar Isi
Pengertian Atom

Sebuah pengertian pasti diawali dengan katanya. Sama halnya dengan atom, kata atom itu sendiri berasal dari bahasa Yunani, atomos. Atomos berarti tidak dapat dibagi-bagi. Sementara itu, pengertian atom-atom menurut para ahli juga berbeda-beda. Berikut pengertian atom menurut para ahli.
1. Leucipus dan Democritus
Atom adalah bagian terkecil dari suatu materi yang tidak dapat dibagi lagi menjadi bagian-bagian tertentu. Atom adalah penyusun segala materi yang ada di dunia ini.
2. John Dalton
Atom adalah partikel terkecil daripada suatu zat yang tidak dapat diuraikan lagi menjadi partikel yang lebih kecil melalui reaksi kimia biasa.
3. Joseph John Thompson
Atom adalah sebuah bola yang bermuatan positif dan dikelilingi oleh elektron seperti kismis.
4. Ernest Rutherford
Atom adalah partikel yang terdiri atas neutron dan proton serta dikelilingi oleh elektron.
Sementara itu, dalam Kamus Besar Bahasa Indonesia (KBBI) atom berarti unsur kimia terkecil (setelah nuklir) yang dapat berdiri sendiri dan dapat bersenyawa dengan yang lain. Bukan hanya itu, dari keempat pengertian atom yang sudah diungkapkan, maka atom dapat diartikan bahwa partikel yang paling kecil dan sudah tidak bisa dibagi-bagi.
“Partikel yang paling terkecil dan tidak bisa dibagi-bagi”, pemikiran ini berasal dari Democritus. Ia adalah ilmuwan pertama yang mengungkapkannya. Pemikiran atau pendapat tentang atom ini bukanlah sebuah penelitian ilmiah, tetapi hanya pemikiran Democritus saja.
Dari pemikiran Democritus, maka banyak ilmuwan yang tertantang untuk meneliti penelitian tentang atom. Bahkan, hingga saat ini, penelitian atom masih berjalan.
Pada umumnya, atom berbentuk seperti lingkaran yang berdiameter 6-30 mm. Gaya elektromagnetik yang ada pada atom dapat mengikat partikel-partikel, seperti proton, neutron, dan elektron.
Terikatnya atom dengan proton, neutron, dan elektron membuat atom dan partikel-partikel tersebut membentuk sebuah molekul. Hingga sampai saat ini, atom belum dapat dilihat oleh berbagai macam alat teknologi.
Inti atom biasa disebut dengan nucleus. Atom mempunyai inti yang dikelilingi dengan elektron, proton, dan neutron. Elektron memiliki muatan negatif. Sedangkan proton mempunyai positif. Setelah sudah ada muatan positif dan negatif, maka neutron dapat dikatakan memiliki muatan yang tidak berpihak pada siapapun, sederhana, neutron bersifat netral.
Perkembangan Atom
Seiring dengan perkembangan ilmu pengetahuan terutama dalam ilmu fisika, sudah ada banyak ilmuwan yang meneliti dan menganalisis teori atom. Ilmuwan-ilmuwan tersebut adalah John Dalton, J.J. Thompson, Ernest Rutherford, dan ilmuwan terakhir yang meneliti atom adalah Niels Bohr.
1. Teori Atom Dalton

John Dalton adalah ilmuwan pertama yang mengembangkan teori atom pada tahun 1803. Teori yang dikembangkan ini merupakan hasil eksperimen John Dalton dalam mengembangkan pemikiran atom Democritus. John Dalton juga beranggapan bahwa atom itu berbentuk seperti bola biliar.
John Dalton beranggapan bahwa atom adalah partikel terkecil yang sudah tidak bisa dibagi-bagi lagi. Dengan kata lain, unsur-unsur yang bergabung dengan atom memiliki komposisi yang tetap.
Secara garis besar, teori atom John Dalton, sebagai berikut:
a) Atom adalah bagian terkecil dari suatu materi yang sudah tidak bisa dibagi-bagi.
b) Partikel-partikel penyusun atom mempunyai zat yang sama.
c) Atom unsur tertentu tidak bisa berubah menjadi atom unsur lain.
d) Dua atom atau lebih dapat bersenyawa atau bereaksi membentuk molekul.
e) Dalam reaksi kimia, perbandingan antara atom-atom penyusunnya memiliki perbandingan tertentu dan sederhana.
Meskipun John Dalton bisa dikatakan sebagai ilmuwan pertama yang mengembangkan teori atom, tetapi teori ini masih memiliki beberapa kekurangan, di antaranya:
a) Seiring dengan perkembangan teori atom, ternyata atom bisa diubah menjadi atom unsur lainnya dengan reaksi nuklir. Dalam hal ini, membuktikan bahwa anggapan John Dalton tentang atom tidak bisa diciptakan ataupun dimusnahkan adalah salah.
b) Dengan adanya isotop, maka anggapan John Dalton tentang atom pada suatu unsur mempunyai kesamaan dalam berbagai hal tidaklah benar. Isotop membuktikan bahwa atom yang sama akan mempunyai kesamaan pada nomor atom, tetapi nomor massanya berbeda.
c) Seiring dengan perkembangan teori atom, sudah banyak ditemukan senyawa dengan perbandingan bilangan yang tidak bulat dan tidak sederhana. Dengan hal ini, maka bisa dikatakan bahwa teori John Dalton yang mengungkapkan bahwa perbandingan unsur dalam suatu senyawa memiliki perbandingan yang bulat dapat dipatahkan.
Pada tahun 1886, telah ditemukan partikel listrik yang bermuatan positif atau yang saat ini dikenal dengan nama proton. Penemu dari partikel listrik ini adalah seorang ilmuwan yang bernama Eugene Goldstein.
Kemudian pada tahun 1897, Thomson menemukan partikel yang memiliki muatan negatif yang saat ini dinamakan elektron. Lalu pada tahun 1932, penemuan partikel dengan muatan netral adapun yang menemukan partikel ini adalah James Chadwick.
Partikel proton, elektron, dan neutron yang telah ditemukan dapat mematahkan teori atom John Dalton yang menyatakan atom sudah tidak bisa dibagi-bagi. Hal ini bisa dikatakan bahwa salah satu kekurangan dari teori atom John Dalton.
Seperti yang sudah dibahas bahwa teori atom John Dalton memiliki cukup banyak kekurangan. Meskipun cukup banyak kekurangan dari teori atom miliknya, tetapi John Dalton tetap dianggap sebagai bapak pencetus teori atom modern.
2. Teori Atom Thomson
 Pada tahun 1987, teori John Dalton tentang bentuk atom seperti bola biliar sudah dipatahkan dengan teori atom yang diciptakan oleh Joseph John Thomson. Ia telah menemukan yang namanya elektron yang saat ini dikenal dengan nama teori atom Thomson.
Pada tahun 1987, teori John Dalton tentang bentuk atom seperti bola biliar sudah dipatahkan dengan teori atom yang diciptakan oleh Joseph John Thomson. Ia telah menemukan yang namanya elektron yang saat ini dikenal dengan nama teori atom Thomson.
Pada teori atom Thomson, atom digambarkan seperti roti kismis. Mengapa atom diibaratkan seperti roti kismis? Karena Thomson beranggapan bahwa atom yang memiliki muatan positif dikelilingi oleh elektron yang bermuatan negatif.
Penemuan partikel subatom yang bermuatan negatif yang dilakukan oleh Thomson dapat mematahkan teori atom John Dalton terutama tentang atom yang tidak memiliki subatom. Dengan kata lain, teori atom Thomson membuktikan bahwa atom masih memiliki sub-partikel atau sub-atom.
Dalam mengembangkan teorinya, Thomson menyatakan bahwa secara keseluruhan atom itu bersifat netral. Hal ini dikarenakan elektron dengan muatan negatif membutuhkan partikel lain yang bermuatan positif yang berfungsi untuk menetralkan muatan negatif yang ada pada atom.
Secara garis besar, teori atom yang diungkapkan oleh Joseph John Thomson dapat disimpulkan menjadi beberapa hal, yaitu:
a) Atom bukanlah bagian terkecil dari suatu partikel.
b) Secara keseluruhan, atom mempunyai sifat yang netral.
c) Massa elektron lebih kecil daripada massa atom.
d) Atom yang bermuatan positif akan tersebar ke seluruh atom, lalu dinetralkan oleh elektron-elektron.
e) Atom yang bermuatan netral memiliki muatan positif dan muatan negatif yang sama. Dengan kata lain, tidak ada muatan positif atau muatan negatif yang berlebihan pada suatu atom.
Hal sangat disayangkan dari teori Thomson adalah tidak ada yang mengembangkan teori ini. Bahkan, teori Thomson mengalami ketidakcocokan pada teori atom miliki Ernest Rutherford. Teori atom milik Ernest Rutherford membuktikan bahwa muatan positif pada atom tidak tersebar merata.
Dengan kata lain, muatan positif pada atom hanya terpusat di bagian tengah atom sehingga dinamakan inti atom.
Salah satu kelemahan lainnya, Teori atom Thomson tidak dapat menjelaskan muatan positif dan muatan negatif pada atom. Selain itu, Joseph John Thomson belu tahu bahwa di dalam atom itu sendiri terdapat yang namanya inti atom.
Hal yang paling berharga dan sangat bermanfaat dari teori atom Thomson adalah Thomson berhasil membuktikan bahwa ada partikel lain yang bermuatan negatif pada atom. Selain itu, dengan teori Thomson ini, kita jadi tahu bahwa atom itu bersifat netral atau jumlah muatan positif dan muatan negatif seimbang.
3. Teori Atom Rutherford
 Ernest Rutherford adalah fisikawan yang lahir di Selandia Baru yang merupakan murid Joseph John Thomson. Dengan penelitian yang dilakukan oleh Rutherford, ia dapat menjawab semua kelemahan yang ada pada teori atom sebelumnya, yaitu teori atom Thomson.
Ernest Rutherford adalah fisikawan yang lahir di Selandia Baru yang merupakan murid Joseph John Thomson. Dengan penelitian yang dilakukan oleh Rutherford, ia dapat menjawab semua kelemahan yang ada pada teori atom sebelumnya, yaitu teori atom Thomson.
Lebih tepatnya pada tahun 1910, Rutherford dan bersama dengan dua asistennya berhasil menemukan inti atom yang memiliki jari-jari lebih kecil daripada atomnya. Teori milik Rutherford ini berasal dari eksperimen penembakan inti atom lempengan emas dengan partikel alfa (sebuah partikel dengan massa empat kali massa atom hidrogen dan muatan positif sebesar dua kali.
Eksperimen penembakan atom dinamakan menjadi Geiger-Marsdeng. Nama pada percobaan itu bisa dikatakan sebagai salah bentuk apresiasi dari Rutherford pada kedua asistennya. Mereka berdua atau asisten Rutherford bernama lengkap, Hans Geiger dan Ernest Masrreden.
Pada saat itu, Rutherford membuat rancangan atau sketsa bersama dua asistennya untuk menembak atom emas oleh partikel alfa yang dipancarkan oleh unsur radioaktif. Dari percobaan ini, sinar radioaktif dapat dibelokkan, diteruskan, dan dipantulkan. Namun, dari hasil percobaan yang telah dilakukan terdapat fakta bahwa ada partikel alfa yang dibelokkan dengan sudut antara 900 sampai 1800.
Berdasarkan penelitian atau percobaan yang dilakukan maka dapat disimpulkan bahwa jika partikel alfa mengenai inti atom, maka bisa terjadi tumbukan yang akan mengakibatkan pembelokan atau pemantulan partikel alfa. Terjadinya hal itu dapat disebabkan karena adanya massa dan muatan atom yang terpusat di inti atom (nukleus).
Dengan hal ini, Rutherford beranggapan bahwa muatan inti atom sebanding dengan massa atom dalam sma (satuan massa atom). Selain itu, hasil dari percobaan dari Rutherford juga mematahkan gagasan Thomson yang menyatakan bahwa atom seperti roti kismis dengan elektron tersebar merata di seluruh bagian atom.
Secara garis besar, teori atom Rutherford dapat dibagi menjadi beberapa poin, yaitu:
a) Atom tersusun dari inti atom (nukleus) dan elektron yang mengitarinya.
b) Muatan positif atau massa atom terpusat di dalam inti atom.
c) Atom bersifat netral. Hal ini dikarenakan jumlah muatan yang ada pada inti atom sama dengan jumlah muatan elektron.
d) Penyebaran partikel alfa tidak dipengaruhi oleh awan elektron.
e) Sebagian besar volume atom adalah sebuah ruang kosong (bukan pejal) karena jari-jari inti atom jauh lebih kecil dari jari-jari atom.
Meskipun teori atom Rutherford merupakan perbaikan dari teori atom Thomson, tetapi pada teori Rutherford masih ada beberapa kekurangan. Salah satu kekurangan dari teori Thomson adalah dalam hal lintasan elektron.
Dengan teorinya, Rutherford mengatakan bahwa elektron itu mengitari inti atom pada lintasan yang relatif jauh dari inti. Dari pernyataan ini, maka teorinya dianggap bertentangan dengan teori elektrodinamika klasik Maxwell.
4. Teori Atom Bohr
Pada saat itu, para ilmuwan sepakat dengan hasil penelitian yang dilakukan oleh Rutherford. Hal yang disetujui oleh para ilmuwan pada saat itu ialah atom terdiri dari inti atom dan elektron yang mengitarinya.
Namun, karena pada lintasan elektron yang diterapkan oleh Rutherford masih memiliki kekurangan, maka seorang fisikawan asal Denmark dan peraih Nobel Fisika tahun 1922 yang bernama Niels Bohr memperbaiki teori atom Rutherford.
Ia melakukan serangkaian percobaan atau penelitian hanya untuk menyempurnakan teori atom Rutherford. Niels Bohr menggunakan model atom nuklir dan teori kuantum Planck untuk menyempurnakan teori atom Rutherford. Hingga saat ini teori atom ini dikenal dengan teori atom Bohr.
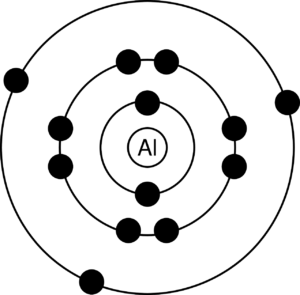
Secara sederhana, model atom milik Niels Bohr hampir mirip dengan perputaran planet yang mengitari tata surya. Oleh karena itu, teori ini juga dikenal dengan nama “model atom miniatur tata surya Niels Bohr”.
Setelah melakukan penelitian atau percobaan, akhirnya Niels Bohr menemukan hasil bahwa elektron-elektron mengitari inti atom yang terdiri dari proton dan neutron pada lintasan-lintasan tertentu, biasaya disebut dengan kulit elektron atau tingkat energi.
Setelah elektron itu pindah dari kulit satu ke kulit lainnya, pasti akan disertai dengan penyerapan sejumlah energi tertentu. Jika dijelaskan secara sederhana, terdapat perpindahan ke kulit lebih luar dan perpindahan ke kulit lebih dalam.
Perpindahan ke kulit lebih luar, tingkat energi lebih tinggi disertai penyerapan energi. Sedangkan, perpindahan ke kulit lebih dalam, tingkat energi lebih rendah disertai dengan pelepasan energi.
Jika diambil secara garis besar, teori atom Niels Bohr terdapat beberapa poin-poin penting, di antaranya:
a) Adanya lintasan stasioner yang memiliki energi tertentu. Lintasan stasioner adalah lintasan-lintasan tertentu tanpa membebaskan energi yang diputari oleh inti atom.
b) Tidak ada energi dalam bentuk radiasi yang dipancarkan atau diserap ketika elektron berada dalam lintasan stasioner.
c) Apabila elektron menyerap energi dari luar, maka elektron itu akan naik ke kulit yang lebih tinggi, lalau akan kembali pada kulit yang semula dengan memancarkan energi radiasi.
d) Elektron dapat berpindah dari satu lintasan ke lintasan lainnya. Jika elektron berpindah dari lintasan dengan energi rendah ke lintasan dengan energi tinggi. Saat terjadi perpindahan, elektron akan menyerap energi dan jika sebaliknya elektron akan menyerap energi.
e) Salah satu kelemahan yang pada teori Niels Bohr adalah tidak dapat menjelaskan spektrum atom yang lebih besar daripada hidrogen. Bukan hanya itu, teori atom Niels Bohr juga tidak bisa menjelaskan efek Zeeman, yaitu spektrum atom yang lebih rumit jika atom diletakkan pada medan magnet.
5. Teori Mekanika Kuantum
Kelemahan yang ada pada teori atom Niels Bohr akhirnya disempurnakan oleh seorang fisikawan dari Austria. Ia adalah peraih Nobel Fisika pada tahun 1933 dan nama fisikawan itu adalah Erwin Schrodinger.
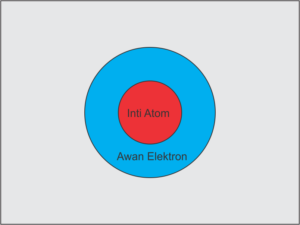
Erwin Schrodinger membuat teori mekanika kuantum atau yang saat ini dikenal dengan “model atom modern”. Teori atom ini menggambarkan sifat pergerakan serta posisi elektron yang berdasarkan pada hipotesis Broglie dan Werner Heisenberg.
Menurut Louis de Broglie, elektron memiliki sifat dualisme, yaitu bukan hanya sebagai partikel, tetapi juga sebagai gelombang. Sedangkan hipotesis Werner Heisenberg merupakan ketidakpastian sifat elektron.
Dengan hipotesis Broglie dan Heisenberg, maka Erwin Schrodinger berhasil menemukan sebuah persamaan gelombang gerakan elektron dalam suatu atom. Rumusan ini dapat menerangkan bahwa lintasan elektron adalah sebuah ruang bukan berupa garis saja.
Secara ringkas, teori atom Erwin Schrodinger atau “model atom modern” memiliki beberapa hal penting, yaitu
a) Atom mempunyai kulit yang di mana setiap kulitnya dan subkulit.
b) Lintasan elektron adalah sebuah ruang bukan berupa garis.
c) Gelombang adalah pergerakan elektron dalam lintasannya.
d) Kedudukan elektron tidak bisa ditentukan dengan pasti.
e) Kecepatan pancaran gelombang disebabkan oleh osilator-osilator yang menentukan pancaran foton oleh sumbernya.
f) Atom-atom yang bergerak sebagai osilator akan menghasilkan gelombang elektromagnetik yang dibarengi dengan frekuensi gelombang yang khusus bagi atom yang bersangkutan.
Baca juga artikel terkait “Pengertian Atom dan Teori Perkembangannya” :
- Sumber Daya Alam Non Hayati
- Sumber Daya Alam Hayati
- Sumber Energi Alternatif
- Sumber Energi Gerak
- Sumber Energi Panas
- Sumber Daya Alam Mineral
- Hujan Asam
- Proses Terjadinya Hujan
- Daur Hidup Nyamuk
- Daur Hidup Katak
- Pemanasan Global
- Penyebab Terjadinya Banjir
- Penyebab Pencemaran Udara
- Penyebab Pencemaran Tanah
- Penyebab Pencemaran Air